Безопасный общедоступный состав для травления меди
Re: Безопасный общедоступный состав для травления меди
Проще разводить. Зачем лимонку лишнюю тратить.
Re: Безопасный общедоступный состав для травления меди
а можно ли обычной водой разводить? не дистиллированной.
Be sincere
Re: Безопасный общедоступный состав для травления меди
Я что-то пропустил и существует обязательное требование разводить исключительно дистиллятом?
Re: Безопасный общедоступный состав для травления меди
дистилятом, только если хранить в дальнейшем перекись.
а перед употреблением можно и из-под крана воду брать
а перед употреблением можно и из-под крана воду брать
Re: Безопасный общедоступный состав для травления меди
Прошу прощения, но статья - бред. Ключевые ОВР неверны, вывод совершенно ошибочен. Кислота вообще как таковая не участвует в реакции и как следствие может быть абсолютно любой, лишь бы ее соль меди была растворима, в качестве окислителя - травителя может быть любое вещество с неустойчивым атомом кислорода: Cu+[O] ->CuO, а CuO+2[H]->[Cu2+]+H2O. К примеру в "марганцовке", "белизне", продувая через раствор озон или просто воздух компрессором можно добиться тех же результатов, но с различной скоростью.
При травлении "медным купоросом" на самом деле травится хлорной медью в присутсвии кислорода воздуха, поваренная соль там вообще не участвует - можно легко проверить взяв чистый CuCl2! Рекомендую! Раствор легко регенерируется, а для ускорения, поскольку основной компонент кислород - продувать воздух, или увеличить поглощаемую поверхность раствора с помощью вибрации (20-40мин вместо 6-8ч!!!), а заготовку располагайте на самом верху - где растворенного кислорода больше всего. Заготовку можно прилепить пластилином/оконной замазкой к пенопласту и пустить плавать по раствору.
При травлении "медным купоросом" на самом деле травится хлорной медью в присутсвии кислорода воздуха, поваренная соль там вообще не участвует - можно легко проверить взяв чистый CuCl2! Рекомендую! Раствор легко регенерируется, а для ускорения, поскольку основной компонент кислород - продувать воздух, или увеличить поглощаемую поверхность раствора с помощью вибрации (20-40мин вместо 6-8ч!!!), а заготовку располагайте на самом верху - где растворенного кислорода больше всего. Заготовку можно прилепить пластилином/оконной замазкой к пенопласту и пустить плавать по раствору.
- mr_kot
- Друг Кота
- Сообщения: 4625
- Зарегистрирован: Пт ноя 27, 2009 18:12:27
- Откуда: Черкассы, UA
- Контактная информация:
Re: Безопасный общедоступный состав для травления меди
Мимикроид писал(а):Прошу прощения, но статья - бред.
Напишите свою, а читатели проверят и оценят. Зачем же гадить в чужой теме, тем более, что методика многими проверена и с успехом используется?
Мимикроид писал(а): При травлении "медным купоросом" на самом деле травится хлорной медью в присутсвии кислорода воздуха, поваренная соль там вообще не участвует - можно легко проверить взяв чистый CuCl2!
Да неужели?
А откуда в медном купоросе хлорид-ионы? Поделитесь своими познаниями.
Re: Безопасный общедоступный состав для травления меди
Написать статью? А зачем? Я уже все написал. Нагадил? Где? Назвал статью бредом? А как еще можно ЭТО назвать, когда формулы неверны, да и травить перекисью и ее солями тоже не открытие. Подобран растворитель для окисной пленки? И это не новость, ее можно и комплексообразователями растворять без кислот. А так, травильный состав вполне рабочий, но он достаточно дорог, медленен, неуправляем и одноразовый (ионы меди, железа, марганца и т.д. каталитически разлагают все виды перекисей). И если нравится – пользуйтесь на здоровье, я не запрещаю, просто предупреждаю новичков.
Ну и напоследок: медный купорос, и травление "медным купоросом" понятия разные. Первое это реактив Cu2SO4*5H2O, а второе название (взято в кавычки!) состава травления, в контексте, купорос с хлорсодержащей солью (можно взять KCl, CaCl2 сути не меняет). CuSO4+2NaCl <-> CuCl2+Na2SO4 и травящая составляющая CuCl2. Ни глауберова соль, ни ее составляющие ионы не участвует в процессе.
Ну и напоследок: медный купорос, и травление "медным купоросом" понятия разные. Первое это реактив Cu2SO4*5H2O, а второе название (взято в кавычки!) состава травления, в контексте, купорос с хлорсодержащей солью (можно взять KCl, CaCl2 сути не меняет). CuSO4+2NaCl <-> CuCl2+Na2SO4 и травящая составляющая CuCl2. Ни глауберова соль, ни ее составляющие ионы не участвует в процессе.
Re: Безопасный общедоступный состав для травления меди
Мимикроид писал(а):Прошу прощения, но статья - бред. Ключевые ОВР неверны, вывод совершенно ошибочен.
А мужики-то не знали...

- mr_kot
- Друг Кота
- Сообщения: 4625
- Зарегистрирован: Пт ноя 27, 2009 18:12:27
- Откуда: Черкассы, UA
- Контактная информация:
Re: Безопасный общедоступный состав для травления меди
Мимикроид писал(а):да и травить перекисью и ее солями
Соли перекиси - это что-то новенькое
Можно пару примеров для неграмотных?
Мимикроид писал(а):в контексте, купорос с хлорсодержащей солью
Мимикроид писал(а):поваренная соль там вообще не участвует
Ну так определитесь наконец то, участвует соль или нет?
Re: Безопасный общедоступный состав для травления меди
Как пожелаете: Na2O2, CaO2, K2O2... Ещё надо?
Поваренная соль является хлорсодержащей, но не все хлорсодержащие являются поваренными, будте внимательнее!
Поваренная соль является хлорсодержащей, но не все хлорсодержащие являются поваренными, будте внимательнее!
Re: Безопасный общедоступный состав для травления меди
Тема: Безопасный общедоступный состав для травления меди.
Порядок безопасности по статье: хлорная медь, хлорное железо, перекись, персульфаты. Перекись - то далеко не на первом месте, а если учесть, что в результате травления образуются соли меди, то хлорная медь вообще в неконкуренции!
Порядок доступности: хлорная медь, перекись, хлорное железо, персульфаты. И опять обман! Хлорную медь можно вплоть до бесплатного сделать самому.
Прошло несколько лет, мужики как не знали, так до сих пор в пролете - обсуждают довольно опасный, и относительно доступный состав...
Порядок безопасности по статье: хлорная медь, хлорное железо, перекись, персульфаты. Перекись - то далеко не на первом месте, а если учесть, что в результате травления образуются соли меди, то хлорная медь вообще в неконкуренции!
Порядок доступности: хлорная медь, перекись, хлорное железо, персульфаты. И опять обман! Хлорную медь можно вплоть до бесплатного сделать самому.
Прошло несколько лет, мужики как не знали, так до сих пор в пролете - обсуждают довольно опасный, и относительно доступный состав...
Re: Безопасный общедоступный состав для травления меди
Да ваще... 
http://pcbdesigner.ru/pcb/travlenie-pec ... -medi.html
Так что вы уж как-нибудь сами...
А мужики-то снова не знали... https://ru.wikipedia.org/wiki/%D0%A1%D0%BE%D0%BB%D0%B8

http://pcbdesigner.ru/pcb/travlenie-pec ... -medi.html
1. Низкая скорость травления.
2. Образование осадка.
3. Вязкая масса в травильной машине.
4. Желтые или белые осадки на медной поверхности.
Так что вы уж как-нибудь сами...
Мимикроид писал(а):Как пожелаете: Na2O2, CaO2, K2O2... Ещё надо?
А мужики-то снова не знали... https://ru.wikipedia.org/wiki/%D0%A1%D0%BE%D0%BB%D0%B8
- mr_kot
- Друг Кота
- Сообщения: 4625
- Зарегистрирован: Пт ноя 27, 2009 18:12:27
- Откуда: Черкассы, UA
- Контактная информация:
Re: Безопасный общедоступный состав для травления меди
Мимикроид писал(а):Как пожелаете: Na2O2, CaO2, K2O2...
Извините, но это не соли, это пероксиды.
И получается пероксид натрия сжиганием натрия в атмосфере кислорода, а не взаимодействием натрия с перекисью:
https://ru.wikipedia.org/wiki/Пероксид_натрия
Получение[править | править вики-текст]
Пероксид натрия образуется при сгорании натрия в кислороде:
А соли - это немного другое:

https://ru.wikipedia.org/wiki/Соли
Мимикроид писал(а):Поваренная соль является хлорсодержащей, но не все хлорсодержащие являются поваренными, будте внимательнее!
Не надо съезжать с темы.
Я уже понял, что из Вас химик, как из го*на пуля. Можете продолжать гадить.
Но лучше для этого создать свою тему и гадить в ней.
Re: Безопасный общедоступный состав для травления меди
Справочно: Автор статьи Дипломированный специалист в области химии. Причём Диплом Белорусского Государственного Университета, Химический факультет.
Желание автора изложить текст в максимально доступном формате, это стандартный приём преподавателя.
А так - любую статью можно бредом назвать))) Безо-основательно и бездоказательно.
Желание автора изложить текст в максимально доступном формате, это стандартный приём преподавателя.
А так - любую статью можно бредом назвать))) Безо-основательно и бездоказательно.
Re: Безопасный общедоступный состав для травления меди
Orion33:
1. Скорость можно повысить. Решение приводил.
2. И? Он вам мешает? В моем решении никакой роли не играет, либо решение с этого сайта - растворять кислотой.
3. Вы травите машинами? Какая вязкость для радиолюбителя?
4. На плата медь стравливается до конца, какие осадки? Ну а если так, воспользуйтесь нашатырным спиртом - он растворяет все соединения меди.
Та да, пока к этому составу не пришел травил чем попало, рецепты составлял из всего что под руку попадалось...
mr_kot:
Значит, вы умеете пользоватся интернетом! Тогда я удивлен, что вы не почитали про перекись, я для вас нашел ссылочку
http://ru.wikipedia.org/wiki/Перекись_водорода
более того по солям:
2NaOH+H2O2=Na2O2+2H2O - похоже на определение солей?
или вытеснение слабой кислоты более сильной:
Na2O2+H2SO4=Na2SO4+H2O2, так что не надо про пули...
ko666ka:
И чего? Вы думаете у меня меньшая квалификация? Это для вас не видно, а мне сразу в глаза бросается.
А проверить очень просто - научным методом:
Отрезаем одинаковые кусочки от медной проволоки без покрытия, бросаем в раствор перекиси с лимонкой и замеряем время до полного растворения. Потом лимонку заменяем на серную, той же концентрации, для чистоты экперимента, растворяем - результат будет похож. Теперь возьмем какой нибудь другой окислитель и проведем те же опыты, а вот здесь время изменится в разы. Вывод: скорость травления не зависит от типа кислоты и зависит только от окислителя. Проверьте сами - вывод статьи и результаты опыта абсолютно противоположны, что ставит под сомнение ваши справочные данные....
1. Скорость можно повысить. Решение приводил.
2. И? Он вам мешает? В моем решении никакой роли не играет, либо решение с этого сайта - растворять кислотой.
3. Вы травите машинами? Какая вязкость для радиолюбителя?
4. На плата медь стравливается до конца, какие осадки? Ну а если так, воспользуйтесь нашатырным спиртом - он растворяет все соединения меди.
Та да, пока к этому составу не пришел травил чем попало, рецепты составлял из всего что под руку попадалось...
mr_kot:
Значит, вы умеете пользоватся интернетом! Тогда я удивлен, что вы не почитали про перекись, я для вас нашел ссылочку
http://ru.wikipedia.org/wiki/Перекись_водорода
более того по солям:
2NaOH+H2O2=Na2O2+2H2O - похоже на определение солей?
или вытеснение слабой кислоты более сильной:
Na2O2+H2SO4=Na2SO4+H2O2, так что не надо про пули...
ko666ka:
И чего? Вы думаете у меня меньшая квалификация? Это для вас не видно, а мне сразу в глаза бросается.
А проверить очень просто - научным методом:
Отрезаем одинаковые кусочки от медной проволоки без покрытия, бросаем в раствор перекиси с лимонкой и замеряем время до полного растворения. Потом лимонку заменяем на серную, той же концентрации, для чистоты экперимента, растворяем - результат будет похож. Теперь возьмем какой нибудь другой окислитель и проведем те же опыты, а вот здесь время изменится в разы. Вывод: скорость травления не зависит от типа кислоты и зависит только от окислителя. Проверьте сами - вывод статьи и результаты опыта абсолютно противоположны, что ставит под сомнение ваши справочные данные....
Re: Безопасный общедоступный состав для травления меди
А вообще, если честно, я никогда не рассматривал перекисный состав как перспективный, да и как его усовершенствовать не представляю возможным, но если поможет, могу немного разъяснить ситуацию.
Основа реакции: H2O2+Cu=CuO+H2O – в идеале на каждые 34г перекиси приходится 64г меди, но ионы меди ее каталитически разлагают, так что в реале меньше. В перекись для продажи добавляют ингибиторы-стабилизаторы уменьшающие влияние каталитических ионов, разумеется, они слабые, да и смысла искать более сильный ингибитор нет, иначе сама основная реакция тоже замедлится. Единственное что приходит на ум – сразу выводить ионы меди из раствора внешним электролизом, т.е. в травильной ванне разместить в сторонке угольные электроды и подать на них напряжение в 0,4-0,5В (ЭП у меди меньше 0,4В значит напряжение нужно не меньше, а ОВП пероксид-иона больше 0,6В – напряжение д.б. меньше этого значения), по крайней мере КПД раствора должно повысится. Не знаю, но может и сработает, пробуйте…
Основа реакции: H2O2+Cu=CuO+H2O – в идеале на каждые 34г перекиси приходится 64г меди, но ионы меди ее каталитически разлагают, так что в реале меньше. В перекись для продажи добавляют ингибиторы-стабилизаторы уменьшающие влияние каталитических ионов, разумеется, они слабые, да и смысла искать более сильный ингибитор нет, иначе сама основная реакция тоже замедлится. Единственное что приходит на ум – сразу выводить ионы меди из раствора внешним электролизом, т.е. в травильной ванне разместить в сторонке угольные электроды и подать на них напряжение в 0,4-0,5В (ЭП у меди меньше 0,4В значит напряжение нужно не меньше, а ОВП пероксид-иона больше 0,6В – напряжение д.б. меньше этого значения), по крайней мере КПД раствора должно повысится. Не знаю, но может и сработает, пробуйте…
Re: Безопасный общедоступный состав для травления меди
Мимикроид писал(а):Он вам мешает?
Нет, мне не мешает - я персульфатом травлю

Мимикроид писал(а):2NaOH+H2O2=Na2O2+2H2O - похоже на определение солей?
или вытеснение слабой кислоты более сильной:
Na2O2+H2SO4=Na2SO4+H2O2, так что не надо про пули...
Нет, не похоже. Соли должны еще диссоциировать в воде на анионы и катионы, а не разлагаться необратимо, а также участвовать в реакции обмена со щелочами и другими солями. В любимой Вами Википедии сказано, что пероксиды металлов МОЖНО назвать солями, но к международной номенклатуре это не имеет никакого отношения.
- mr_kot
- Друг Кота
- Сообщения: 4625
- Зарегистрирован: Пт ноя 27, 2009 18:12:27
- Откуда: Черкассы, UA
- Контактная информация:
Re: Безопасный общедоступный состав для травления меди
Мимикроид писал(а):более того по солям:
2NaOH+H2O2=Na2O2+2H2O - похоже на определение солей?
Химик, зачем формулу наизнанку вывернул?
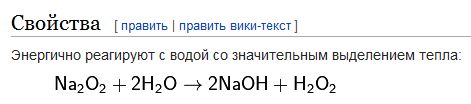
Умный, да?
Я заканчиваю это бесполезное переливание из пустого в порожнее. Дальше без меня.
Re: Безопасный общедоступный состав для травления меди
Orion33 писал(а):Разница в цвете указывает на то, что образуются разные катионы меди. Cu+ имеет зеленый цвет
Cu+ бесцветный и в растворе не существует.
Orion33 писал(а):Cu2+ - синий. Думаю, что более сильное окисление происходит за счет большего кол-ва окислителя в растворе, т.е. перекиси.
Cu2+ тоже бесцветен. чтобы убедиться - прокалите медный купорос. получится совершенно белое вещество. все окрашенные соли меди - комплексные соединения.
а крепкий раствор CuCl2 - ярко зелёный потому, что помимо аквакомплексов меди там еще есть хлоридные и аквахлоридные. в школах такому не учат. Вам следует убавить менторский тон.Orion33 писал(а):Ошибаетесь. Водный раствор окрашивают ионы, а не вещества. CuCl2 при диссоциации в воде распадается на Cu2+ и 2Cl-. Ионы Cl- получаются и при диссоциации поваренной соли, раствор которой прозрачный. А цвет ионов Cu2+ - синий, как у медного купороса, потому как при диссоциации последнего получаются такие же ионы меди.
кислый цитрат меди.a5021 писал(а):Кстати упомянуть, в хранящемся у меня отработанном растворе выпали голубые хлопья, которые более в воде не растворяются. Есть подозрение, что это именно цитрат меди. Оставшаяся жидкость имеет насыщено-зеленый цвет. Вот бы еще знать, что это такое. Хлорид?
а, что касается карбамида, то он, помимо бокового потрава, способен предотвращать некоторые неприятные побочные реакции в этой системе. возможно, что это полезная добавка.
это может закипеть, и надо будет убегать.DJ_URAN писал(а):Други! А если раствор перекиси не 3%, а 6%? Делать концентрированный (то есть лимонки и соли в двукратном объеме)? Или разводить перекись?
Последний раз редактировалось Murlock Пт май 08, 2015 19:39:34, всего редактировалось 1 раз.
" Если на небе есть ангелы, то, их небесное воинство построено на принципах мафии"
У.Н. Румфорд.
----------------------------------------
http://www.youtube.com/watch?v=qWfIYU9Zzs4 А.К. "Легион"
У.Н. Румфорд.
----------------------------------------
http://www.youtube.com/watch?v=qWfIYU9Zzs4 А.К. "Легион"
Re: Безопасный общедоступный состав для травления меди
голословненько. может предложите свои?Мимикроид писал(а):Ключевые ОВР неверны
очень бы хотелось посмотреть на сам процессМимикроид писал(а):К примеру в "марганцовке"
ооо! а почему не хлор или фтор?Мимикроид писал(а):продувая через раствор озон
т.е. хлорид меди(II) принципиально не годитсо?Мимикроид писал(а):в качестве окислителя - травителя может быть любое вещество с неустойчивым атомом кислорода: Cu+[O] ->CuO
на воздухе - да, в растворе нет. очевидно, Вы ничего не знаете про двойной электродный слой в месте контакта металла и раствора электролита. ну, да ладно.Мимикроид писал(а):Cu+[O] ->CuO
травится и в отсутствие кислорода воздуха. факт. сможете объяснить?Мимикроид писал(а):При травлении "медным купоросом" на самом деле травится хлорной медью в присутсвии кислорода воздуха
ну, рекомендовать промышленный метод легко и приятно.Мимикроид писал(а):можно легко проверить взяв чистый CuCl2! Рекомендую!
Мимикроид писал(а):Ну и напоследок: медный купорос, и травление "медным купоросом" понятия разные. Первое это реактив Cu2SO4*5H2O, а второе название (взято в кавычки!) состава травления, в контексте, купорос с хлорсодержащей солью (можно взять KCl, CaCl2 сути не меняет)
тут был применён очень "научный" метод получения данного вывода - умозрительный. и, разумеется, вывод получился неверный. почитайте вику по данной выше ссылке.Мимикроид писал(а):Отрезаем одинаковые кусочки от медной проволоки без покрытия, бросаем в раствор перекиси с лимонкой и замеряем время до полного растворения. Потом лимонку заменяем на серную, той же концентрации, для чистоты экперимента, растворяем - результат будет похож.
цитрат-ион сам является неплохим выводителем, пряча медь от перекиси в глубь довольно большой своей молекулы. а про электролиз - мне понравилось. сюда еще можно добавить экстракцию ионселективными краунэфирами. или абсорбцию хелатными ионитамиМимикроид писал(а):Единственное что приходит на ум – сразу выводить ионы меди из раствора внешним электролизом
ну и зря! тут веселоmr_kot писал(а):Я заканчиваю это
" Если на небе есть ангелы, то, их небесное воинство построено на принципах мафии"
У.Н. Румфорд.
----------------------------------------
http://www.youtube.com/watch?v=qWfIYU9Zzs4 А.К. "Легион"
У.Н. Румфорд.
----------------------------------------
http://www.youtube.com/watch?v=qWfIYU9Zzs4 А.К. "Легион"

